
近日,上海临床研究中心/上海科技大学生物医学工程学院程登峰教授联合罗宗化教授团队,在药学领域国际权威期刊《Acta Pharmaceutica Sinica B》(影响因子14.6)发表题为“Preclinical evaluation of a novel tetrazine probe within a pretargeted delivery system for theranostics in HER2-positive tumor-bearing mice models”的研究论文。该研究围绕HER2阳性肿瘤的精准诊疗需求,构建了一种基于生物正交点击化学的预定位放射性核素递送系统,为HER2阳性实体瘤的高对比度显像和安全有效治疗提供了新的策略。

HER2是多种实体瘤中的重要分子靶点。近年来,针对HER2的核医学诊疗研究持续推进,但传统的抗体直接放射性标记策略仍面临一些瓶颈,例如抗体体内循环时间长、背景清除慢、正常组织辐射暴露较高等问题,这些因素在一定程度上限制了其进一步转化应用。
针对这一问题,研究团队利用IEDDA介导的预定位策略(图1)。与传统“直接标记”的方式不同,预定位策略先将经过修饰的抗体输送至肿瘤部位,待其在体内完成富集并从非靶组织中逐步清除后,再给予带有放射性的四嗪小分子探针,使其与肿瘤部位预先富集的抗体快速发生点击反应,从而实现放射性信号在肿瘤内的精准沉积。相比直接标记抗体,这一策略有望在保证肿瘤靶向性的同时,降低正常组织不必要的辐射暴露,提升成像对比度和治疗安全性。
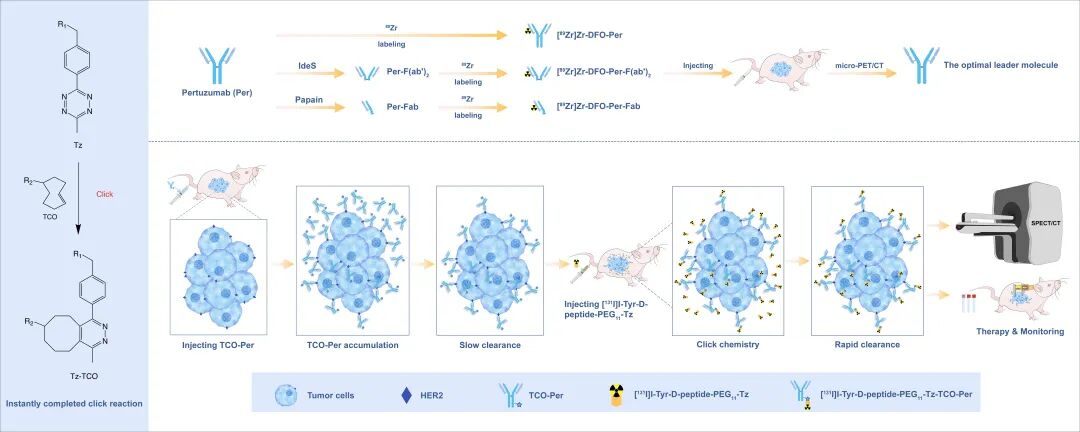
图1 基于Tz探针的HER2预定位诊疗体系作用模式图
本研究的核心亮点之一,在于新型Tz探针[131I]I-Tyr-D-peptide-PEG11-Tz的设计与构建。四嗪(Tetrazine, Tz)是整个预定位体系中的关键效应分子,直接决定了后续点击反应的实现效率以及体内递送效果。研究团队围绕Tz探针的反应性能、体内稳定性和分布特征进行了系统优化,构建出兼具点击能力与体内应用潜力的新型探针分子。
从结构上看该探针主要由三部分组成(图2):一部分为负责与TCO修饰抗体发生点击反应的四嗪基团;一部分为用于改善亲水性和体内行为的PEG11及D型多肽序列;另一部分则为用于放射性核素标记的酪氨酸位点。这样的结构设计,使该探针不仅能够实现高效点击,还兼顾了体内稳定性、可标记性和药代动力学特征,为预定位体系的实际应用提供了重要支撑。
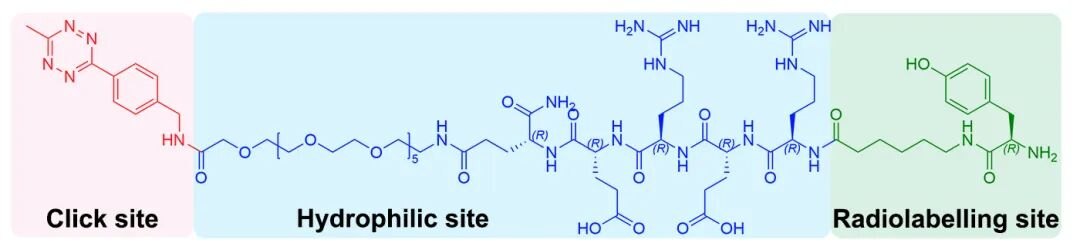
图2 新型Tz探针前体Tyr-D-peptide-PEG11-Tz设计图
在此基础上,研究团队进一步完成了先导抗体筛选和预定位条件优化,并在HER2高表达荷瘤模型中验证了该体系的应用潜力(图3)。研究结果表明,这一新型Tz探针在预定位体系中能够实现良好的肿瘤靶向递送,并表现出快速背景清除、较高成像对比度和较好的治疗潜力,体现了预定位策略在HER2阳性肿瘤诊疗一体化中的优势。更为重要的是,新型Tz探针的开发不仅是预定位体系中的一个技术环节,更是提升整个诊疗体系性能的关键所在。通过对Tz探针进行针对性优化,有望进一步改善放射性药物在体内的递送效率和安全性,为HER2阳性肿瘤乃至更多实体瘤的精准核医学诊疗提供新的工具和思路。
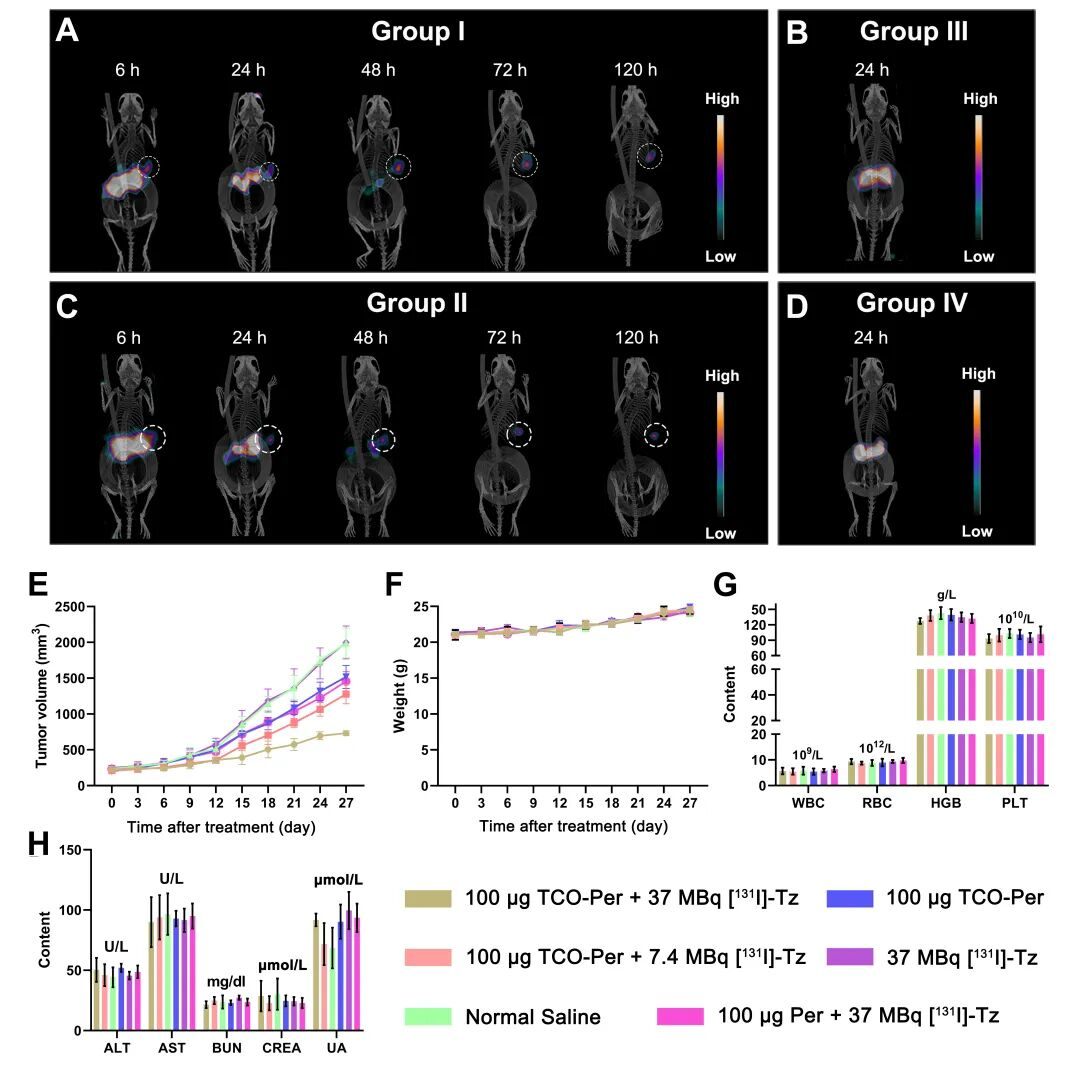
图3 新型Tz探针在HER2阳性荷瘤模型中的显像与治疗效果
总体而言,该研究成功构建并验证了一种新型的靶向HER2的预定位诊疗一体化体系,其显示出良好的成像与治疗应用前景。该工作不仅为生物正交点击化学在核医学中的应用提供了新的实验依据,也为预定位诊疗策略的进一步优化和临床转化奠定了基础。
上海临床研究中心核医学科程登峰教授、复旦大学附属中山医院核医学科石岱博士、上海科技大学罗宗化教授为论文共同通讯作者。复旦大学附属中山医院2022级博士研究生马鹏程、复旦大学附属中山医院核医学科谭辉副主任医师、上海临床研究中心核医学科林卿玉副研究员为论文共同第一作者。
文章链接:https://doi.org/10.1016/j.apsb.2026.03.004