
心肌梗死后,心脏会经历由炎症、细胞死亡和纤维化瘢痕形成等驱动的不良重塑,最终导致心力衰竭。然而,驱动过程中的细胞和分子机制一直未被完全阐明。近日,上海临床研究中心特聘科学家、上海科技大学生命科学与技术学院张辉教授团队与同济大学唐娟教授团队联合在《循环》(Circulation)发表一项突破性研究,首次系统揭示了P16阳性细胞在心脏不良重塑中的关键作用,并提出了靶向CCL8信号或P16阳性成纤维细胞的精准干预新策略,为开发基于免疫调节和细胞精准治疗的新型心梗药物提供了重要的理论基础。

团队利用先进的细胞谱系标记技术为细胞“贴标签”,首次绘制了心梗后心脏中P16阳性细胞的“身份图谱”。研究发现,在受损的心脏区域,成纤维细胞、巨噬细胞、血管内皮细胞甚至心肌细胞都会大量表达P16。团队锁定了其中两类关键细胞——P16阳性的成纤维细胞和巨噬细胞——它们并非旁观者,而是主动“煽风点火”的“肇事者”。这两种类型细胞大量分泌趋化因子CCL8,将细胞毒性淋巴细胞——尤其是CD8+ T细胞(杀伤性T细胞),招募至受损的心脏组织。这些被招募来的免疫细胞释放攻击性分子,直接导致心肌细胞凋亡,进一步加剧组织结构破坏和功能障碍(图1)。
为了验证这一机制,团队在小鼠模型中开展了系列干预实验。结果表明,无论是使用抗体中和CCL8,还是利用Cre/loxP技术条件性敲除P16阳性细胞中的Ccl8基因,均可显著减少细胞毒性淋巴细胞的浸润、保护心肌细胞、缩小心梗后瘢痕面积,并有效改善心脏功能(图1)。
更值得关注的是,团队采用“双重锁定”基因技术(双重组酶介导的白喉毒素受体表达系统),实现了对P16阳性成纤维细胞或巨噬细胞的精准清除。结果显示,仅清除P16阳性成纤维细胞即可显著促进心脏修复;而清除P16阳性巨噬细胞则无明显效果,提示P16阳性成纤维细胞是驱动不良重塑的核心细胞亚群,也是未来药物干预的精准靶点。
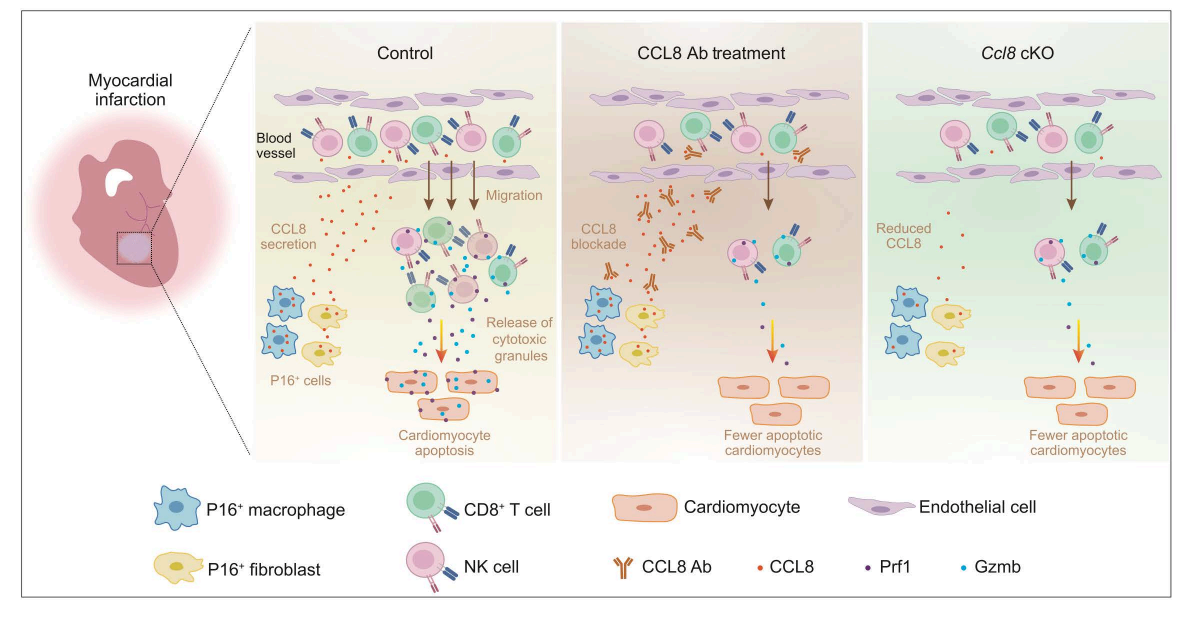
图1.研究示意图:P16阳性细胞通过分泌CCL8招募CD8+ T细胞和自然杀伤(NK)细胞,诱导心肌细胞凋亡,推动心梗后心脏不良重塑。
“过去我们只知道P16阳性细胞与衰老相关,但对其在心脏病后的具体功能知之甚少。”论文通讯作者张辉教授表示,“本研究不仅明确了它们的身份,还揭示了它们如何与免疫系统‘联手’加剧损伤。这提示我们,治疗心梗或许不需要‘地毯式轰炸’般地清除所有衰老细胞。通过阻断CCL8信号或精准清除P16阳性成纤维细胞,我们有望在干预的同时减少对正常细胞的误伤,实现更安全、更高效的治疗。”
上海科技大学生命科学与技术学院博士研究生严磊、郑嘉蕾和同济大学博士后卢正开为本文共同第一作者。张辉教授和唐娟教授为共同通讯作者。上海科技大学为论文第一单位,上海临床研究中心为共同完成单位。
论文链接:https://doi.org/10.1161/CIRCULATIONAHA.125.077172