
在最新的《Bioorganic Chemistry》期刊中,由上海科技大学免疫化学研究所、复旦大学附属中山医院的科研团队共同发表了一项开创性研究成果:“Discovery of a first-in-class protein degrader for the c-ros oncogene 1 (ROS1)”。团队成功开发了首个针对ROS1融合蛋白的蛋白降解剂,这一发现有望彻底改变ROS-1融合阳性非小细胞肺癌(NSCLC)的治疗方式。
ROS1是一种在人类癌症中频繁出现突变的受体酪氨酸激酶,其融合突变与非小细胞肺癌(NSCLC)等多种疾病的发展密切相关。当前临床针对这种融合蛋白多采用靶向抑制剂,如crizotinib和entrectinib等进行治疗。然而,这些抑制剂面临着抗药性发展的挑战,其中一种解决方案是使用蛋白降解技术(PROTAC)来降解并清除ROS1融合蛋白,从而彻底阻断其信号传导,杀死癌细胞。
本研究的开创性意义和优势在于:1)全球首发:SIAIS039作为首个针对c-ros原癌基因1(ROS1)的蛋白降解剂,开启了靶向治疗的新篇章。2)高效降解:与传统的ROS1抑制剂不同,SIAIS039通过PROTAC(蛋白降解靶向嵌合体)技术,彻底降解ROS1融合癌蛋白,有效阻断其激酶活性,增强了抗肿瘤潜力。
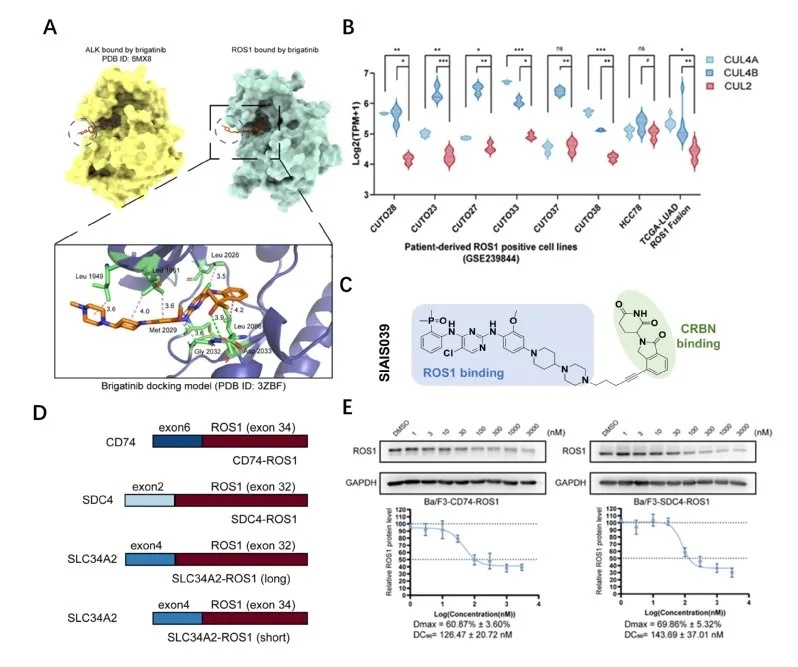
图1:ROS1蛋白降解剂的分子设计和降解活性。A:分子对接显示链接子引入位点B:常见E3连接酶在ROS1阳性肺癌细胞中的表达;C: ROS1降解剂SIAIS039;D:肺癌中部分常见的ROS1融合模式;E:降解剂对两种常见ROS1融合蛋白的降解效果。
本研究的主要亮点如下:1)创新机制:利用分子对接和合理设计,SIAIS039展现了对多种ROS1融合癌蛋白的高效降解能力(图1)。2)长效作用:SIAIS039展示出其持久的蛋白降解效果,通过阻断癌细胞信号通路,有效抑制肿瘤生长。3)卓越疗效:体外实验显示,SIAIS039的抗肿瘤效果超越了目前获批的两种药物crizotinib和entrectinib(图2A-B)。4)高生物利用度:在小鼠异种移植模型中,SIAIS039展现了良好的口服生物利用度和抗肿瘤活性,同时没有明显毒副作用,为其临床应用提供了广阔前景(图2C)。
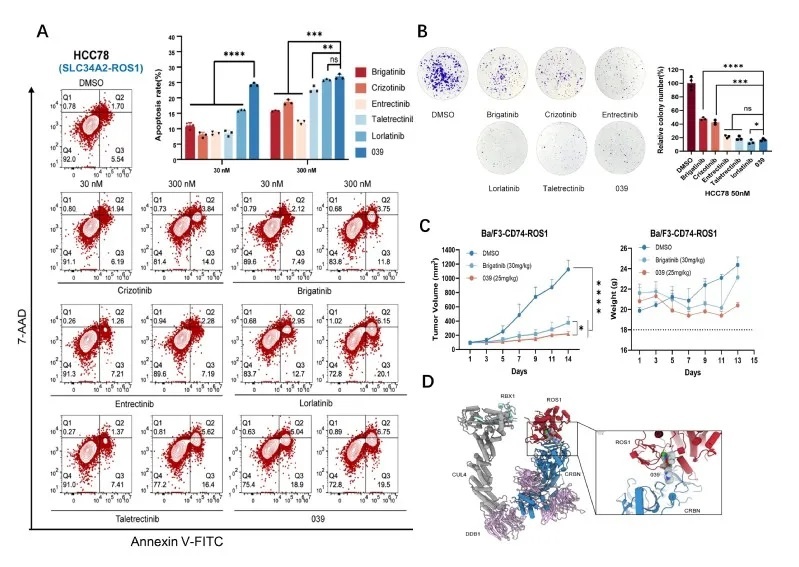
图2 ROS1蛋白降解剂的体内外抗肿瘤活性
A:细胞凋亡实验;B:抑制克隆形成;C:高效抑制肿瘤生长;D:降解作用模式图
该降解剂的开发为ROS1融合阳性非小细胞肺癌(NSCLC)患者提供了新的治疗选择,为使用传统疗法无效的患者提供了新的希望,同时,其研制还为未来基于PROTAC的药物设计提供了重要的参考和蓝图。该研究的成功不仅展现了通过靶向降解蛋白质来治疗癌症的巨大潜力,也预示着新的医学时代的到来。随着靶向降解蛋白技术的不断研究和发展,未来几年内,我们可能会看到这种新疗法的临床转化,从而彻底改变癌症治疗的领域。
上海科技大学访问硕士研究生杨镓汶(中山医院)和上海科技大学免化所/生命科学与技术学院博士生吴逸凡为本文共同第一作者。上海科技大学免化所宋肖玲副研究员、姜标教授和中山医院卢春来副主任医师为本文共同通讯作者。本文主要在国家自然科学基金(No. 82072592)和上海市科学技术委员会“科技创新行动计划”(No. 20S11903100)的资助下完成,同时本项目还得到了上海科技大学、上海市科学技术委员会面上自然科学基金项目(No. 21ZR1412600)、上海临床研究中心和上海市生物大分子与精准医药前沿科学研究基地的大力支持。
论文链接:
https://doi.org/10.1016/j.bioorg.2024.107590
(免费全文链接:https://authors.elsevier.com/a/1jLvzAHs8hwrQ,2024年8月20日前有效)