
6月20日,上海科技大学生命科学与技术学院范高峰实验室与合作者在学术期刊《细胞化学生物学》(Cell Chemical Biology)上以封面文章发表题为“NAMPT-targeting PROTAC and nicotinic acid co-administration elicit safe and robust anti-tumor efficacy in NAPRT-deficient pan-cancers”的研究论文,开发了具有更优代谢稳定性的新一代靶向NAMPT(烟酰胺磷酸核糖转移酶)的嵌合体(PROTAC)降解剂,与烟酸联用在治疗NAPRT(烟酸磷酸核糖转移酶)缺陷型泛癌中展示出安全性和有效性。

杂志封面图
NAD+(烟酰胺腺嘌呤二核苷酸)作为氧化还原反应的辅酶,具有参与能量合成和DNA修复等多种生理功能。NAMPT作为合成NAD+补救途径的关键限速酶在多种肿瘤细胞中高表达,是癌症治疗中的潜在靶点。NAMPT一方面在细胞内以iNAMPT的形式发挥酶活功能,负责NAD+的生物合成;另一方面分泌到胞外以eNAMPT的形式发挥非酶活功能,促进肿瘤发生发展。前期靶向NAMPT的策略主要集中在传统酶活抑制剂的开发,但临床上效果不佳。研究团队在先前研究中利用蛋白降解靶向嵌合体技术开发了两种化合物SIAIS630120和SIAIS630121,能够同时降解iNAMPT和eNAMPT两种形式的NAMPT蛋白,但是出现了与传统抑制剂类似的毒性问题。因此,解决靶向NAMPT带来的毒副作用至关重要。
NAD+在机体内一共有三条合成途径,该研究首先验证了多种肿瘤细胞对靶向NAMPT的PROTAC分子的敏感性,发现靶向NAMPT的PROTAC在NAPRT缺陷的肿瘤细胞中具有更好的杀伤效果,提出将NAPRT缺陷的癌症作为靶向NAMPT蛋白的PROTAC分子的适应症,同时联用烟酸 (Nicotinic Acid) 给药以减弱NAMPT靶点的毒副作用。
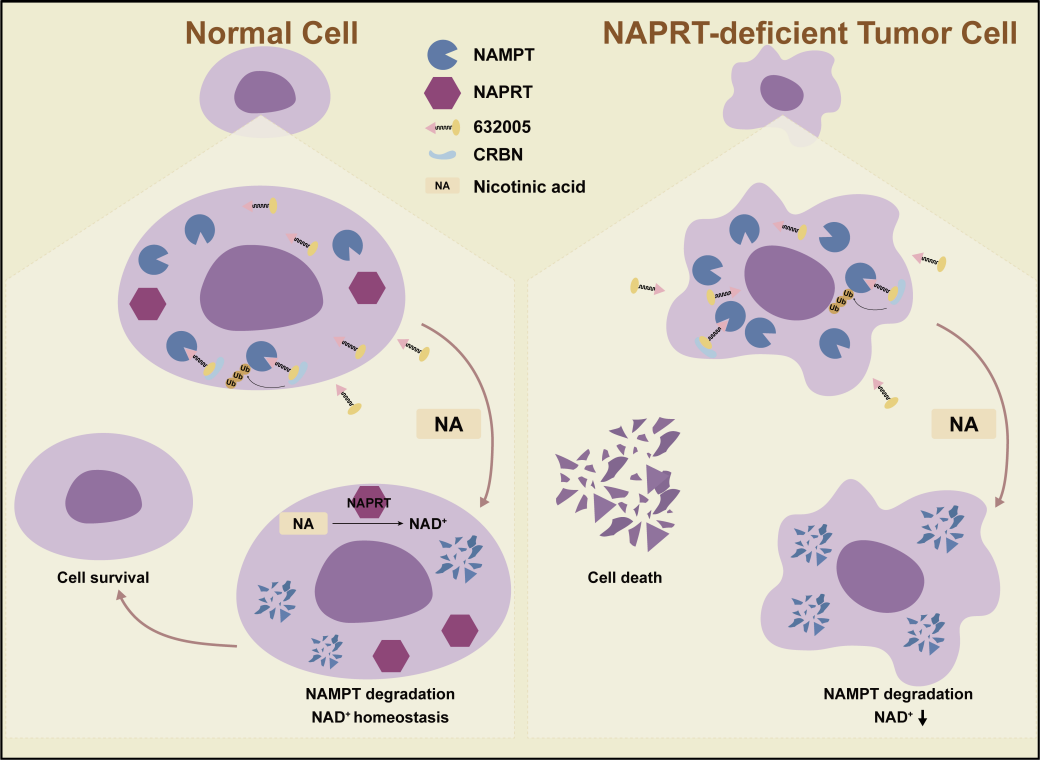
图1. PROTAC联用NA减弱毒性示意图
对已开发的PROTAC分子进行进一步优化得到了代谢稳定性更好的第二代PROTAC分子(632005),证明其在与烟酸联用时,可在体内外有效的减弱靶向NAMPT的毒副作用。为进一步评估联用烟酸给药对PROTAC抗肿瘤作用的影响,研究还构建了血液恶性肿瘤、前列腺癌的异种移植模型以及来源于病人的肝癌PDX模型,证明了靶向NAMPT的PROTAC联用烟酸在NAPRT缺陷的泛癌中具有显著的抗肿瘤效果。
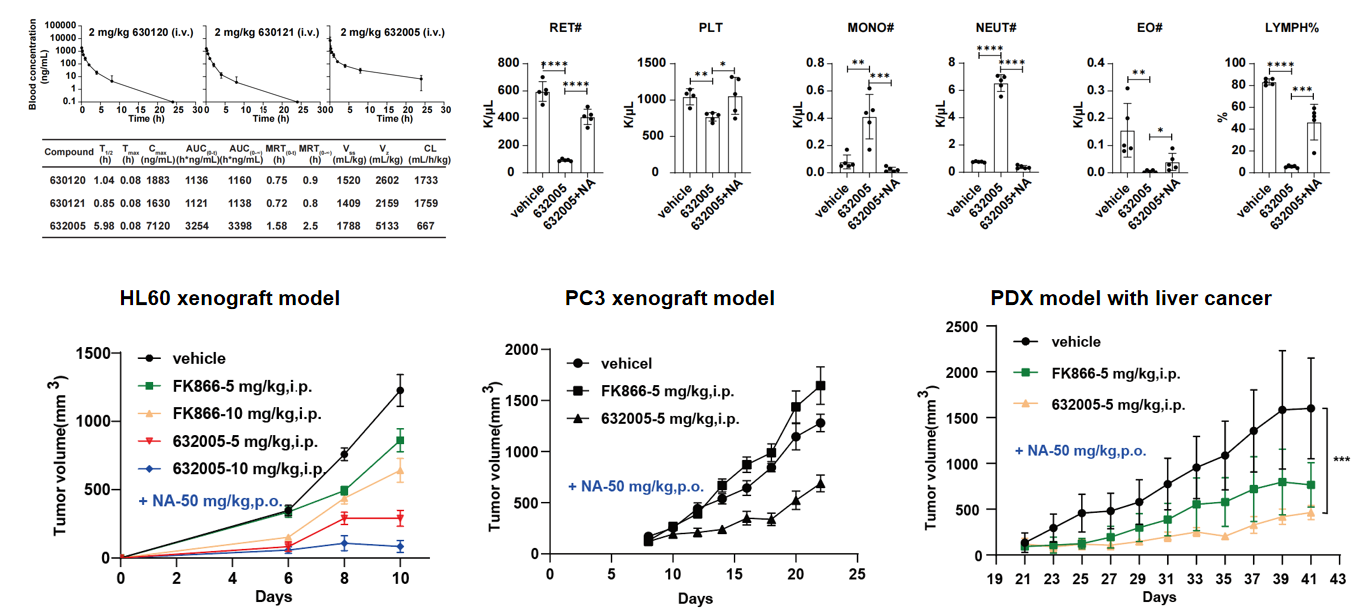
图2. NAMPT-PROTAC联用NA在NAPRT缺陷的泛癌中显示出安全性和有效性
该研究为靶向NAMPT的治疗带来新的希望,并表明第二代PROTAC分子(632005)具有作为癌症治疗的代谢药物的潜力,对未来临床环境中患者的选择以及安全有效的治疗策略的发展具有深远的意义。
上海科技大学生命学院2022级博士研究生朱小童、2022级硕士研究生李椰、物质学院2020级博士研究生刘海霞为共同第一作者。上海临床研究中心特聘科学家、上科大生命学院范高峰、上海交通大学医学院附属第九人民医院徐斌、标新生物医药科技(上海)有限公司杨小宝为本文的共同通讯作者。上海科技大学为第一完成单位,上海临床研究中心为共同完成单位。
论文链接:https://www.cell.com/cell-chemical-biology/fulltext/S2451-9456(24)00208-3